近年来,利用化学方法对多肽和蛋白质进行修饰的报道尽管已经有很多,但对多肽末端氨基进行特异性的识别和修饰却依然极具挑战性。通常而言,当多肽N末端氨基酸的α-碳上有一些活性基团时,可辅助实现氨基的识别,其成功的例子就包括半胱氨酸与醛基反应生成噻唑烷。然而相比于其它19种天然氨基酸,甘氨酸因不含活性侧基,其末端氨基的特异性识别与修饰则更加困难。
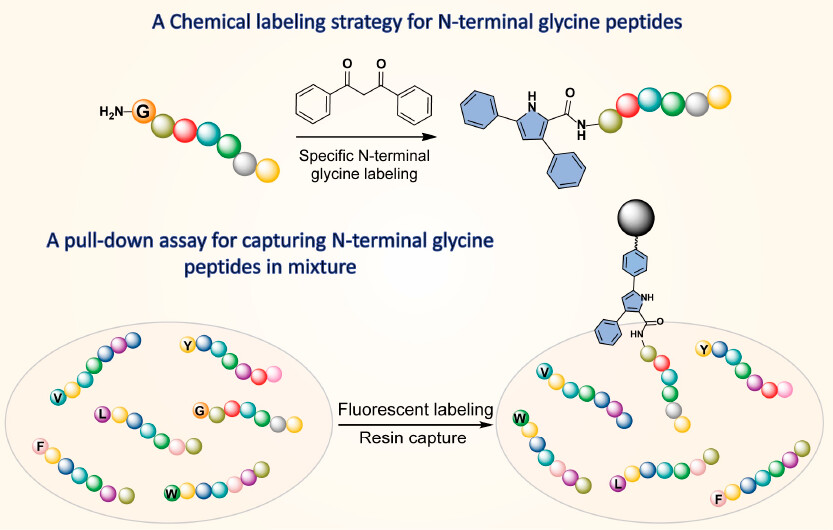
图1.N末端为甘氨酸多肽的特异性荧光修饰示意图
近日,我院刘洪煦副研究员与德克萨斯大学奥斯汀分校的研究人员通过利用甘氨酸的α-亚甲基碳与芳环取代的1,3-二酮的“双重活化”反应实现了N末端为甘氨酸的多肽的特异性修饰(图1),生成含吡咯的荧光产物。除甘氨酸外的其它19种氨基酸由于仅含有α-次甲基(α位有取代基),无法完成“双重活化”,因此不能生成吡咯结构,使得该方法对于N末端为甘氨酸的多肽具有选择性(图2)。
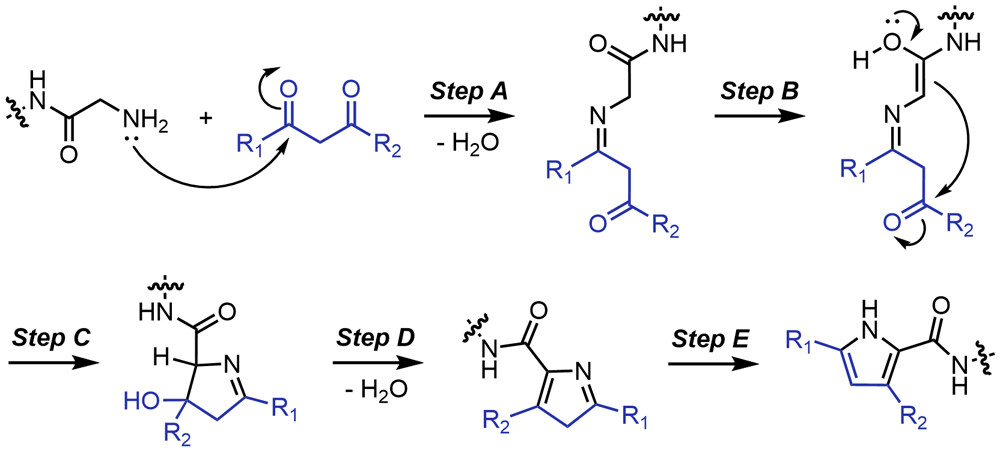
图2.多肽N末端甘氨酸与1,3-二酮的反应机理
本工作首先利用甘氨酸甲酰胺盐酸盐作为研究对象与1,3-二苯基-1,3-丙二酮进行反应,测试了方法的有效性,并通过核磁、质谱和X-射线单晶衍射等表征方法确定了产物为二苯基取代的吡咯衍生物。然后通过紫外可见吸收光谱和荧光光谱等测试,确定了产物可以在367 nm处给出强的荧光。在确定了该方法的可行性后,作者进一步将其用于N末端为甘氨酸的多肽的荧光修饰(图2)。实验结果表明,当肽链中含有赖氨酸、丝氨酸、谷氨酰胺、谷氨酸、天冬氨酸、甲硫氨酸和酪氨酸等具有特殊侧基的氨基酸时,仍体现出良好的修饰效果。当结构中含有半胱氨酸时,可将其巯基用碘乙酰胺保护后参与反应并最终获得目标产物;而当肽链中含有赖氨酸时,其侧链的氨基虽然可以与1,3-二酮反应生成亚胺,但该副产物可以在酸性条件下水解成目标产物。
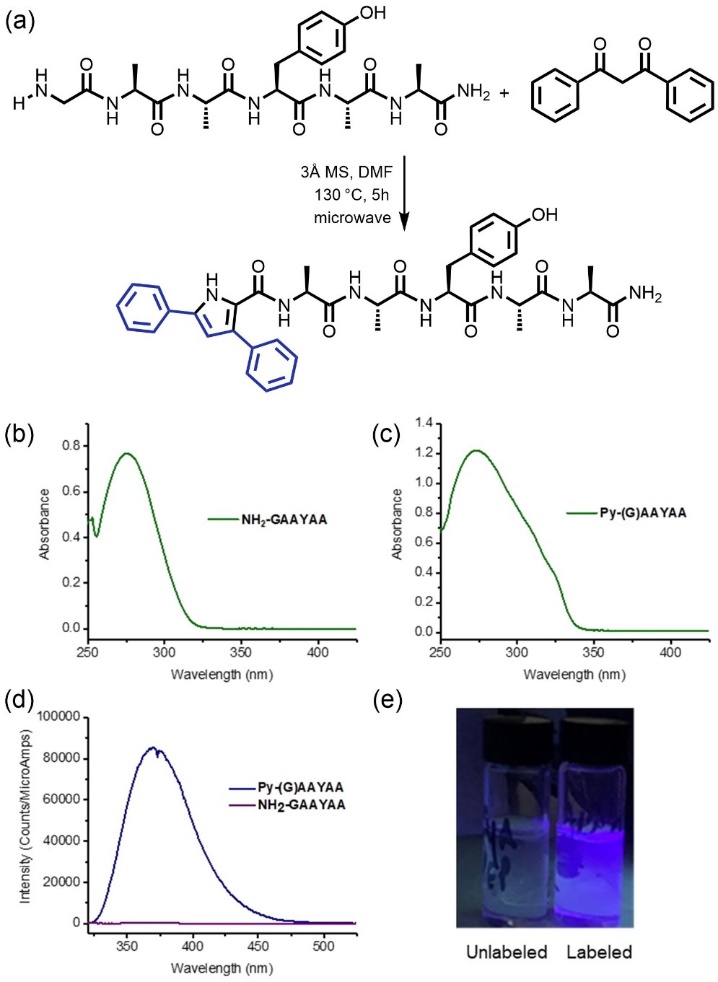
图3.多肽修饰反应及相关的吸收光谱和荧光测试
为验证方法的实用性,作者利用含炔基的1,3-二苯基-1,3-丙二酮与N末端为甘氨酸(G)、苯丙氨酸(F)、缬氨酸(V)、色氨酸(W)、亮氨酸(L)和酪氨酸(Y)的混合多肽体系进行反应。之后,通过在酸性条件下使亚胺水解等一些简单处理后,作者利用叠氮基团修饰的树脂珠粒与产物的炔基发生CuAAC反应,进行了“pull-down”实验,最终将N末端为甘氨酸的多肽特异性地修饰和提取出来。该方法为复杂体系中N末端为甘氨酸的多肽的特异性修饰、捕获和荧光检测提供了一种有效的方法。该工作于近期发表在J. Am. Chem. Soc.上。
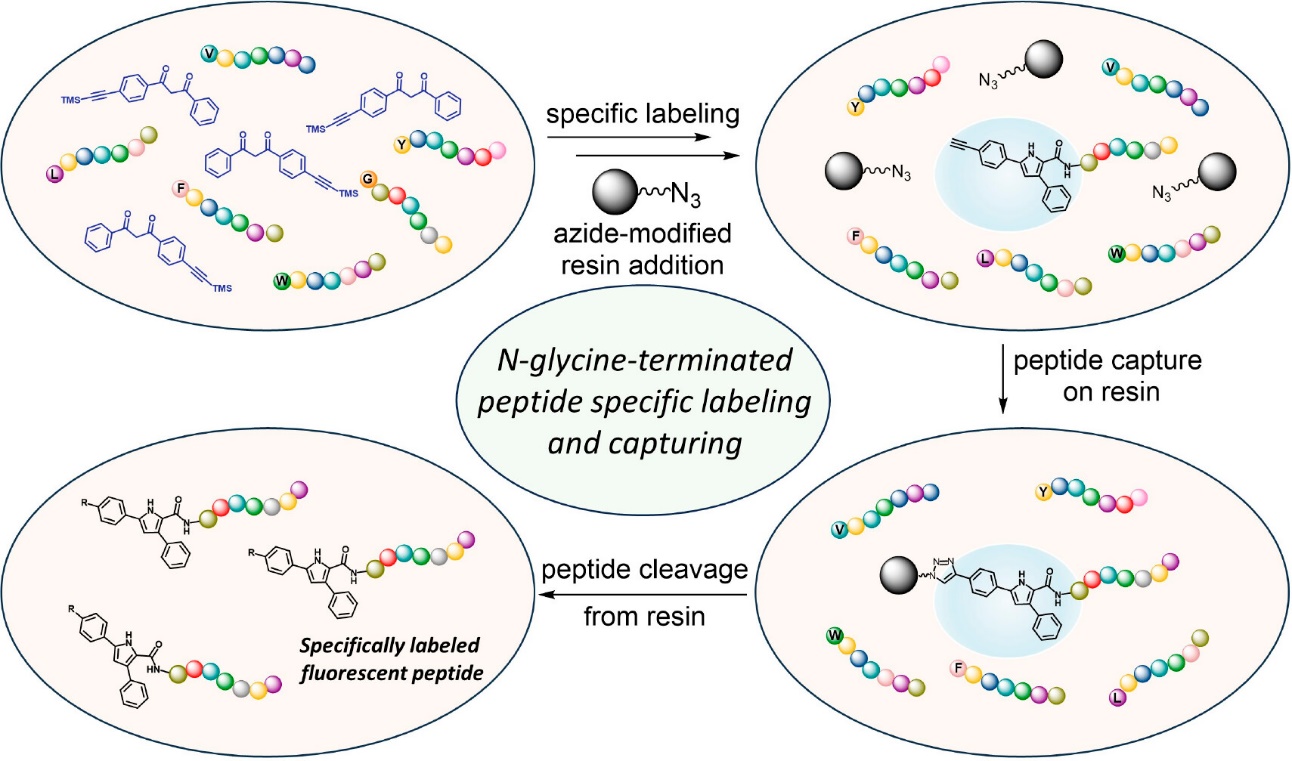
图4. “Pull-down”实验流程示意图
原文链接:https://doi.org/10.1021/jacs.4c04141
撰稿:刘洪煦
编辑:杨燕玲
审核:李乙文