骨关节炎(OA)是一种以软骨退行性病变和滑膜炎症为特征的关节疾病。OA导致的关节稳态失衡会进一步影响软骨的力学耗散与传导、滑液的合成与更新等,从而造成软骨和滑膜损伤,引起关节疼痛与僵硬,严重时甚至会导致骨组织暴露。开发新型润滑体系、重塑软骨润滑功能可以降低磨损和减轻疼痛,从而减缓骨关节炎和抑制骨关节坏死。现有的两性离子聚合物在关节润滑和骨关节炎治疗领域仍然面临诸多亟待解决的问题,例如大量用于OA治疗的材料疗效来自于抗炎药物或促成软骨药物,频繁用药必然会对机体有副作用;单方面对分解代谢的抑制作用对关节稳态的重塑达不到理想的效果等。
近日,我院李建树教授团队以“Mimicking Antioxidases And Hyaluronan Synthase: A Novel Zwitterionic Nanozyme for Photothermal Therapy of Osteoarthritis为题在AdvancedMaterials上报道了一种MoS2基纳米酶(MoS2@PDA–Mg@PSB,MPMP)来实现OA的光热治疗。MPMP可以同时模拟代谢酶和合成酶:(i)模拟以SOD和CAT为代表的抗氧化酶来清除OA环境中的ROS/RNS并且补充O2;(ii)模拟HAS促进滑膜间充质干细胞分泌透明质酸,从而实现内源性增强关节润滑性能。同时,MPMP具有温和的光热转化性能,可以通过局部产热促进HSP 70的表达来进一步增强其类酶活性。因此,MPMP纳米酶在炎症环境下依然可以促进骨髓间充质干细胞的成软骨分化,从而实现软骨修复,以达到更好的OA治疗效果。
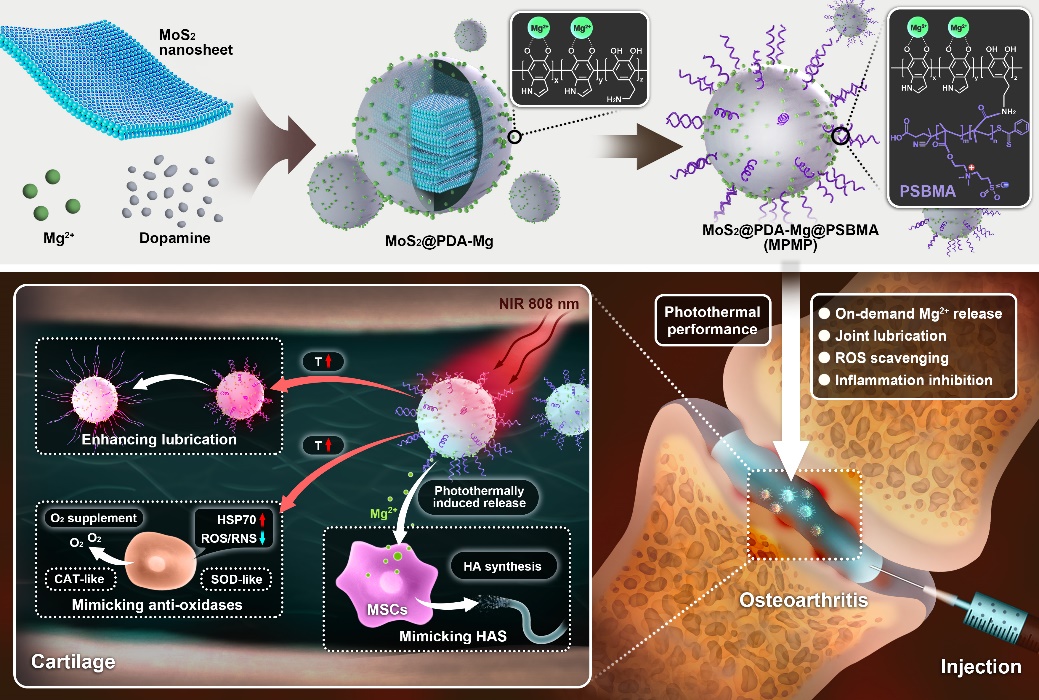
示意图:纳米酶制备过程和作用机理图
研究人员将MoS2纳米片封装于掺镁聚多巴胺的内部,然后在其表面修饰磺酸甜菜碱聚合物,从而制得MPMP纳米酶。这种纳米酶具有稳定的光热转换效率,可以实现Mg2+控释。光热作用一方面可以促进Mg2+按需释放,另一方面可以促进两性离子聚合物克服分子链之间氢键、离子–偶极作用形成的能垒,从而提更好的润滑性能(摩擦系数0.028)。

研究人员进一步分析了MPMP纳米酶的类抗氧化酶活性,发现其对于多种活性氧(H2O2、·OH、O·- 2等)和活性氮具有优异的清除效果,且能够补充O2。MPMP纳米酶对H2O2的亲和力(Km= 10.61mM)和催化速率(0.56mM/min)优于目前报道的具有类CAT活性的纳米催化材料。

通过光热作用,MPMP–NIR可以激活细胞的热休克反应,从而通过HSP70和Mg2+抑制NF–κB、IL–17信号通路,增强MAPK信号通路。因此,MPMP–NIR在抑制细胞炎症反应、氧化应激反应的同时,既可以促进BMSCs的成软骨分化,又可以发挥类透明质酸合成酶活性促进SMSCs合成与分泌透明质酸。


通过MIA诱导的OA小鼠模型,可以证实MPMP–NIR能够抑制关节间隙变窄、减少骨赘生成和抑制关节炎症反应,促进ColII和蛋白多糖的合成与分泌,从而恢复光滑的软骨表层。在治疗早期,MPMP–NIR发挥纳米润滑剂的功能,减缓运动过程中摩擦力造成的软骨磨损;在治疗中后期,MPMP–NIR通过其优异的类抗氧化酶活性清除关节腔内的活性物质,同时,通过激活热休克反应,一方面加速成软骨过程,一方面发挥类透明质酸酶活性促进透明质酸合成,从而补充关节润滑性能。因此,MPMP–NIR可以有效治疗OA,重塑关节稳态。

我院2020级博士生俞鹏为论文第一作者,李建树教授和谢婧副研究员为论文共同通讯作者。该研究工作获得了国家自然科学基金杰出青年基金和面上项目的支持。
论文链接:https://doi.org/10.1002/adma.202303299
撰稿:谢婧
编辑:杨燕玲
审核:刘向阳